患者さん・一般の方へ
治験ってなあに?~新しい「くすり」の誕生~
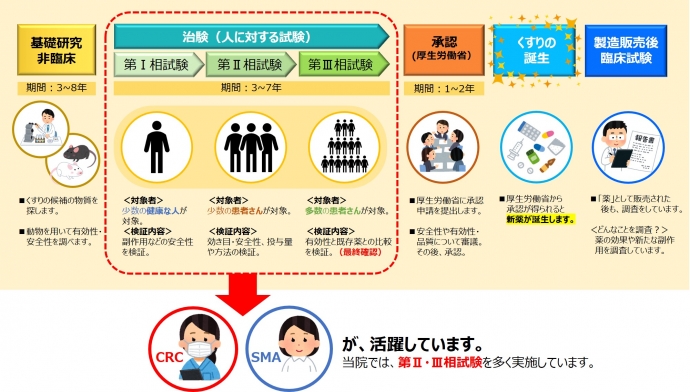
現在、病気の治療にはさまざまな薬が使われています。それらはすべて、国からその使用についての承認を得ているものです。この承認を得るためには「安全に使えるか」、「効き目があるか」また「現在一般的に使用されている薬よりも優れているか」などについて調べた試験の結果を国に提出し、審査を受ける必要があります。これらの試験の中で「ひと」に対して行われる試験のことを「治験」といいます。
治験は、病気で苦しむ患者さんの治療に役立つ、より良い薬を世に出すために必要なものです。
新しい「くすり」が使えるようになるためには、次に示すような決められた手続きや段階を踏む必要があります。
治験は、病気で苦しむ患者さんの治療に役立つ、より良い薬を世に出すために必要なものです。
新しい「くすり」が使えるようになるためには、次に示すような決められた手続きや段階を踏む必要があります。
CRC 【Clinical Research Coordinator】 治験(臨床研究)コーディネーター
SMA 【Site Management Associate】 治験事務局担当者
SMA 【Site Management Associate】 治験事務局担当者
患者さんの安全と人権
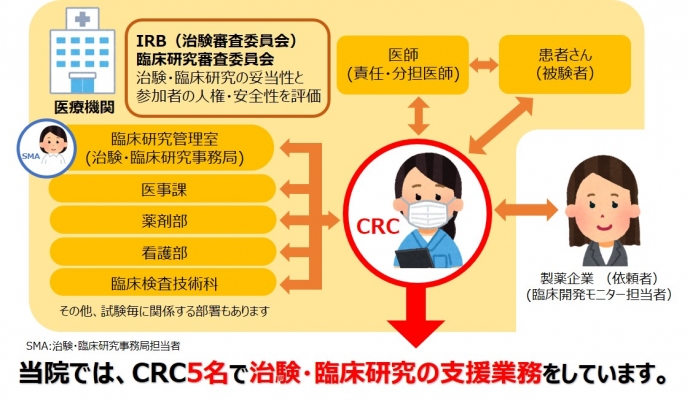
治験は国の定められた厳しいルール「GCP(医薬品の臨床試験の実施に関する基準)」に従って、参加される患者さんの安全と人権の保護に配慮しながら進めていきます。
当院で開催される「治験審査委員会」にて治験の内容を審議し、患者さんの安全と人権を守ります。
当院で開催される「治験審査委員会」にて治験の内容を審議し、患者さんの安全と人権を守ります。
インフォームド・コンセント(説明と十分な情報を共有した合意)
治験を行う医師が、患者さんに説明文書をお渡しします。医師は、「治験の目的・試験内容(検査など)・予想される副作用」について説明をします。 CRC(臨床研究コーディネーター)が説明補助をすることもあります。十分な説明を受けた後、参加するかしないかをご家族と相談するなど十分に考えてから決めることが大切です。治験への参加を決めるのは患者さんです。
治験に参加中、いつでもどんな理由でも辞退することができます。また、参加することを断っても不利益になることは一切ありません。
治験に参加中、いつでもどんな理由でも辞退することができます。また、参加することを断っても不利益になることは一切ありません。
参加条件の確認(検査・診察)
参加条件を満たしているかどうかを確認するための検査や診察を行います。参加条件は参加する試験によって異なり、参加条件をすべて満たす人のみが治験薬の使用を開始できます。
健康被害に対する補償措置について
治験に参加したことによる健康被害が生じた場合は、それに対する適切な処置や治療を受けることができます。補償の内容は治験によって異なりますので、担当医師や担当CRCにお問い合わせください。
当院で治験に参加されている方へ
治験に参加されている間は、スケジュール通りの検査・診察が必要です。
下記のような場合は、担当医師や担当CRC、臨床研究管理室までご連絡ください。
下記のような場合は、担当医師や担当CRC、臨床研究管理室までご連絡ください。
| 予定を変更したい時 |
|---|
| 治験のための来院予定を変更する必要がある時は、説明文書に記載されている担当CRCまでご連絡ください。 |
| 治験を受けている診療科と異なる診療科や、他の病院を受診する時 |
|---|
| 治験薬と併用できない薬や治療法がないか確認する必要があります。 受診する前に、治験担当医師または担当CRCまでご連絡ください。また、他の病院を受診する際には、治験参加時にお渡しした「治験参加カード」を病院の医師・薬局(薬剤師)へご提示ください。 |
治験のQ&A
Q1. 治験に参加した後でも、途中でやめることはできますか?
治験に参加された後でも、途中で治験をやめたいと思ったら、それがどのような理由でも、治験の参加をやめることができます。たとえ途中で治験の参加をやめても、あなたの今後の治療に何らかの不利益を受けることは決してありません。その時の患者さんの状態に一番あった治療を引き続き受けることができます。お気軽に、担当医師や担当CRCにご相談ください。
Q2. プラセボって何ですか?
プラセボとは、見た目は治験薬と同じですが、有効成分は含まれていません。人によってはプラセボであるにも関わらず、効果が出る場合もあります。治験薬の効果と安全性を正確に評価するためにプラセボが使用されることがあります。
Q3. 治験の診察代や検査代はどうなりますか?
治験に参加している間に、飲んでいただく治験のお薬や検査費は、治験を依頼している企業等が負担します。再診料等は、通常の診察の時と同様に患者さんがご負担いただくことになります。
Q4. 治験に参加するメリット・デメリットを教えてください。
メリット
- 新しい治療を受けるチャンスがあります。
- 新しい【くすり】の誕生に協力することで、社会貢献ができます。
- 通常の治療よりも詳細な診察や検査が行われ、病気の状態や検査結果について詳しく説明を受けられます。
- 治療によっては、診察費や検査代がいつもより少なくなる場合や負担軽減費※1が支払われることもあります。
※1 治験参加に伴う入院や来院回数の増加などの負担を軽減するための費用です。
デメリット
- 治療は体調に変化がないか慎重に診察するため、来院や検査の回数が多くなることがあります。
- くすりの飲み方、生活の仕方など、守らなくてはいけないことがあります。
※食べてはいけないものや、一緒に飲んではいけないくすりもあります。 - まれに、これまで知られていなかった副作用が現れることがあります。
CRCは、何をしてくれる人ですか?
CRC 【Clinical Research Coordinator】 治験コーディネーターの略称
臨床研究コーディネーターとも言われています。
責任医師の指示のもと、医学的判断を伴わない治験・臨床研究業務の支援を行います。医師、製薬企業(依頼者)やご協力いただく患者さんの支援、医療機関内の他部署との連携など、治験・臨床研究の実施に必要な調整役としての専門職です。
治験に参加する患者さんの相談窓口として、診察や検査をサポートします。何か分からないことや心配なことがありましたら、遠慮せずにご相談ください。
臨床研究コーディネーターとも言われています。
責任医師の指示のもと、医学的判断を伴わない治験・臨床研究業務の支援を行います。医師、製薬企業(依頼者)やご協力いただく患者さんの支援、医療機関内の他部署との連携など、治験・臨床研究の実施に必要な調整役としての専門職です。
治験に参加する患者さんの相談窓口として、診察や検査をサポートします。何か分からないことや心配なことがありましたら、遠慮せずにご相談ください。
当院CRCの1日を追跡
| 8:15~8:30 | 出勤し、新着メールの確認。 来院予定の患者さんのカルテをチェックします。 |
|---|---|
| ▼ | |
| 8:30~12:00 | 治験に参加している患者さんの対応
実施することもあります。 |
| ▼ | |
| 12:00~13:00 | 昼食 |
| ▼ | |
| 13:00~14:30 | 症例報告書の記載確認、患者さんのカルテチェック、電子症例報告書(EDC)入力、書類保管や治験依頼者との電話・メール確認対応。 |
| ▼ | |
| 14:30~15:00 | ミーティングに参加し、他のCRCと情報共有します。 |
| ▼ | |
| 15:00~16:00 | 検体回収依頼書の回収・保管、次回来院予定者の検査キットの準備。 |
| ▼ | |
| 16:00~17:00 | 医師と、スケジュールの確認や書類チェック。 その他、担当している試験の書類整理・準備やスケジュール調整を行います。 |
| ▼ | |
| 17:00 | 退勤 |
治験相談窓口
臨床研究管理室(治験・臨床研究事務局)では、治験・臨床研究についての疑問、一般的な質問や相談もお受けしますのでお気軽にご相談ください。
※実施中の臨床研究(観察研究)についてのご相談は、情報公開文書に記載のお問い合わせ先にご連絡いただきますようお願いいます。
※実施中の臨床研究(観察研究)についてのご相談は、情報公開文書に記載のお問い合わせ先にご連絡いただきますようお願いいます。
| お問い合わせ先 |
| 磐田市立総合病院 臨床研究管理室 【対応時間】月~金曜日(土・日・祝除く)8時15分から17時00分まで 【TEL】0538-38-5000(代表) 【FAX】0538-38-5029 【Email】E-mail:chiken【※】hospital.iwata.shizuoka.jp (【※】を@に変更してください) ※メールでのお問い合わせについてはお時間を要する場合もあります。お急ぎの場合は対応時間内にお電話ください。 |
